- korrekte Klassifizierung und Risikoklasse nach MDR
- Konformitätserklärung nach Maschineverordnung auch für Sportlaufbänder
Sehr geehrte h/p/cosmos Vertriebs- und Servicepartner,
h/p/cosmos wird dem Slogan „der Zeit Voraus“ (ahead of time) nicht nur bei innovativen Produkten und Technologien gerecht, sondern auch in den relevanten regulatorischen Bereichen zur Erfüllung aller gesetzlichen, normativen und regulatorischen Anforderungen.
Seit 1998 ist h/p/cosmos nach MDD und seit dem Jahr 2022 auch nach MDR durch eine Benannte Stelle zertifiziert.
Das schafft nicht nur Vertrauen, sondern auch Sicherheit für Patienten, Anwender und Händler von Medizinprodukten.
Dieses Dokument aus der Reihe „Regulatory Update“ widmet sich der korrekten Risikoklassifizierung durch die Hersteller, beleuchtet auszugsweise Details der technischen Dokumentation, um allen involvierten Wirtschaftsakteuren, Behörden und Stakeholdern zu ermöglichen die Verantwortungen, notwendigen Aktionen und Risiken entsprechend einzuschätzen, zu planen und durchzuführen.
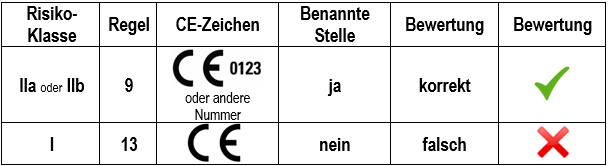
Beim h/p/cosmos International Distributor Meeting IDM 2025 vom 6. bis 9. April 2025 in Schloss Hohenkammer bei München haben wir beim Thema Regulatory Affairs u.a. auch schon berichtet, dass das BfArM in Bonn die von h/p/cosmos schon seit 1998 verwendete Klassifizierungsregel 9 für Laufbänder bestätigt hat, und dass somit jedes Laufband mit Motorantrieb für den medizinischen Bereich ein CE-Zeichen mit 4-stelliger Kennnummer einer benannten Stelle benötigt.
DOWNLOAD
vollständiges Dokument (15 Seiten) mit detaillierter Begründung und jüngsten Gerichtsurteilen bei falscher Risikoklasse
WICHTIG: Laufbänder mit Motorantrieb für Physiotherapie und/oder Diagnostik-Anwendungen sind nach Regel 9 in die Risikoklasse IIa oder IIb zu klassifizieren und eine Benannte Stelle (Notified Body) muss in die Zertifizierung und Überwachung einbezogen sein. Das CE-Zeichen braucht eine 4-stellige Kennnummer der Benannten Stelle.
 |
Aus der MDR ergibt sich, dass eine falsche Klassifizierung eines Medizinproduktes dazu führt, dass das Produkt nicht verkehrsfähig ist und somit auch nicht auf dem Europäischen Markt vertrieben bzw. in Verkehr gebracht werden darf.
Die Anwendbarkeit der Regel 9, resp. die Abgabe oder der Austausch von Energie bei der Anwendung von Laufbänder als Medizinprodukt ergeben sich nicht nur aus der Zweckbestimmung, der Logik und den physikalischen sowie biomechanischen Grundsätzen beim Gehen und Laufen auf dem Laufband, sondern wurden unzählige Male nicht nur durch den Laufband-Hersteller h/p/cosmos sondern u.a. wie folgt von unabhängigen Behörden und/oder Stellen und Experten aus Industrie und Wissenschaft bestätigt:
28.02.2025 / BfArM Bescheid vom 28.02.2025 mit Geschäftszeichen: 91.3.32-5634-K-0049/24
Mit Schreiben vom 11.10.2024 hat h/p/cosmos als Hersteller beim BfArM (Bundesinstitut für Arzneimittel und Medizinprodukte) den Antrag gestellt, auf Grundlage von § 6 Abs. 2 MPDG über die Klassifizierung eines Laufbands mit Motorantrieb und Schnittstelle zu entscheiden.
Das BfArM hat auf Antrag von h/p/cosmos bestätigt, dass bei bestimmungsgemäßer Verwendung des Laufbands ein Energieaustausch mit der Patientin oder dem Patienten stattfindet.
1) Klassifizierungs-Regel 9 ist anwendbar
2) Am Laufband erfolgt eine Abgabe / Austausch von mechanischer Bewegungsenergie
3) Das angefragte Laufband ist in Risikoklasse IIa einzustufen […]
Gekürzter Auszug aus dem BfArM Bescheid vom 28.02.2025 für ein „einfaches und ganz normales“ Laufband ohne robowalk Gangtrainer, ohne Perturbation und ohne hohe Geschwindigkeiten mit den Spezifikationen: Motorantrieb, Lauffläche 150/50 cm, Geschwindigkeit 0 … 22 km/h, Steigungswinkel
0 … 25%, Schnittstelle für EKG und/oder Spiroergometrie, Optional Herzfrequenzmessung durch Zubehör (z.B. POLAR), Optional verstellbare Handläufe, Laufband ohne Messfunktion, Laufband ohne Diagnostikfunktion, Anwendung für Physiotherapie und Diagnostik.
1998 bis 2025 (jedes Jahr) / Benannte Stelle: TÜV SÜD Product Service GmbH, München
Zertifizierungsaudit und jährliches Überwachungsaudit von 1998 nach MDD / MPG und seit 2022 nach MDR / MPDG / ISO 13485 samt Überprüfung der technischen Dokumentation mit Bestätigung zur Anwendbarkeit der Regel 9.
https://www.hpcosmos.com/de/kontakt-support/media-downloads/sicherheit-zertifikate
13.09.2024 / Bayerisches Landesamt für Gesundheit und Lebensmittelsicherheit, München
Freiverkaufszertifikat Nr./No. AP-2697-22-V6032-46309/12024 nach Art. 60 Verordnung (EU) 2017/745 i.V.m. § 10 Medizinprodukte-Durchführungsgesetz (MPDG) in den jeweils geltenden Fassungen zur Vorlage bei den zuständigen Behörden. ... nach jeweiliger Überprüfung der EU – Konformitätserklärungenhttps://www.hpcosmos.com/de/kontakt-support/media-downloads/sicherheit-zertifikate
Auch bestätigt durch Freiverkaufszertifikate / Free Sales Certificates z.B. mit Datum u.a.: 08.05.2002, 28.06.2007, 02.05.2013, 18.07.2014, 01.09.2022, 29.08.2023
18.12.2023 / Paris Lodron Universität Salzburg / Univ.-Prof. Dr. Hermann Schwameder
Stellungnahme zu Austausch bzw. Abgabe von Energie beim Gehen und Laufen auf einem Laufband
Paris Lodron Universität Salzburg, Sport- und Bewegungswissenschaft, Fachbereichsleiter, Leiter AG Biomechanik, Schlossallee 49, 5400 Hallein-Rif, Austria download
30.11.2023 / Universitätsklinikum Halle (Saale) / apl. Prof. Dr. phil. Rene Schwesig
Einschätzung zu Energieaustausch bei Belastungen auf Laufbandergometern
Forschungslaborleiter, MLU Halle-Wittenberg, Medizinische Fakultät, Universitätsklinikum Halle (Saale), Department für Orthopädie, Unfall·und Wiederherstellungschirurgie, Labor für Experimentelle Orthopädie & Sportmedizin, Ernst-Grube-Straße 40, 06120 Halle (Saale) download
13.02.2023 und 04.10.2023 / Dr. Björn Zimmermann / Sportwissenschaftler und Prokurist bei h/p/cosmos
Dr. Zimmermann hat zum Thema Energieübertragung vom elektrisch betriebenen Laufband auf den menschlichen Körper auch ein PDF und ein kurzes Video erstellt. download PDF
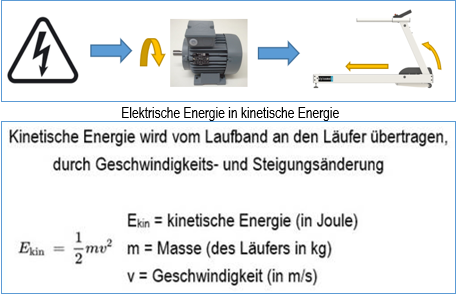
20231004_Energieuebertrag_Laufband_Geschwindigkeit_Steigung.mp4
8. April 2011 / Regierung von Oberbayern – Gewerbeaufsichtsamt München
[…] „Die Klassifizierung von Medizinprodukten folgt prinzipiell den Grundgedanken - je höher das potentielle Risiko für negative Auswirkungen auf den menschlichen Körper, umso höher ist das Medizinprodukt in die entsprechende Klasse einzustufen. Nach den Empfehlungen, auf der Basis üblicher Anwendungen von Medizinprodukten, der Arbeitsgruppen von EUROM VI und F+O werden Laufband-Ergometer in der Liste von Klassifizierungsbeispielen gemäß Abschnitt "Ergometrie" der Klasse IIa zugeordnet.
Abweichend von dieser Einstufung wird, unter Berücksichtigung von Abschnitt II Nr. 2.5 Anhang IX Klassifizierungskriterien 93/42/EWG sowie der von Ihnen geschilderten potentiellen Gefährdung für Patienten im Sinne von Regel 10 - aktive diagnostische Produkte, die speziell für die Kontrolle von vitalen physiologischen Parametern bestimmt sind und bei denen die Art der Änderung zu einer unmittelbaren Gefährdung (gezielt verursachte Herzfunktionsstörung) eines Patienten führen können - Ihre Klassifizierung nach IIb befürwortet.“ […]
Das BfArM prüft zwar keine Produktgruppen sondern jedes Produkt stets im Einzelfall unter Berücksichtigung der jeweiligen Zweckbestimmung und weiterer Leistungsdaten. Die Anwendbarkeit der Regel 9 sowie die Tatsache, dass am Laufband eine Abgabe / Austausch von mechanischer Bewegungsenergie erfolgt, ist nun auch u.a. vom BfArM bestätigt. Ergo geht h/p/cosmos davon aus, dass für alle Laufbänder mit Motorantrieb die Regel 9 gilt, weil physikalische Grundgesetze und biomechanische Prinzipien beim Gehen und Laufen auf einem Laufband unabhängig von Hersteller und Modell identisch sind.
Laufband mit Motor als Medizinprodukt = Klasse IIa oder IIb
Nicht nur h/p/cosmos sondern durchaus auch eine Reihe weiterer Hersteller von Laufbänder halten die gesetzliche und regulatorischen Richtlinien ein. Aber leider nicht alle. Bei h/p/cosmos haben die Testberichte / Nachweisdokumentationen alleine zur Einhaltung der EU Maschinenrichtlinie/Maschineverordnung 30 Seiten. Nur einige Beispiele aus der jüngsten Technischen Dokumentation von h/p/cosmos:
|
|
Testbericht / Nachweisdokumentationen |
Ersteller |
Seiten |
1 |
Klassifizierungsprotokoll nach Konformitätsbewertungs-Verfahren20240619_MDR_classification_protocol_treadmill_ klassifizierungsprotokoll_laufband.pdf |
h/p/cosmos |
24 |
2 |
Grundlegende Anforderungen nach Maschinerichtlinie 2006/42/EG resp. EU Maschinenverordnung 2023/123020240615_ER_acc_to_MR_2023_1230_hpcosmos_ treadmill_family_150_50_G7_signed.pdf |
h/p/cosmos |
30 |
3 |
Grundlegende Sicherheits- und Leistungsanforderungen nach MDR (EU) 2017/745 GSPR general safety and performance requirements20240618_ER_acc_to_MDR_EU_2017_745_hpcosmos_ treadmill_150-50_G7_unfiltered_signed.pdf |
h/p/cosmos |
58 |
4 |
Engineering Testplan20240614_cos31000_hpcosmos_150-50_G7_pluto_ mercury_Engineering_Testplan_signed_Gate_3.pdf |
h/p/cosmos |
18 |
5 |
Gerätespezifikationen der Modelle dieser Gerätefamilie
|
h/p/cosmos |
40 |
| 6
|
Testbericht mechanische Sicherheit stationäre Trainingsgeräte / Laufbänder nach EN ISO 20957-1 / EN 957-620240603_treadmill_hpcosmos_150-50_G7_cos31032-0001_ IEC60601-1_TUEV_713311665_100_ISO20957-6_EN957-6_TECHNICAL_REPORT.pdf |
DAkkS akkreditiertes und unabhängiges Testlabor |
29 |
7 |
Risikomanagement Akte / Risk management file all h/p/cosmos treadmill families according DIN EN ISO14971 incl. Plan, Residual Risk & Report20250310_hpcosmos_risk_management_file_all_ treadmills_1.14_signed.pdf |
h/p/cosmos |
1579 |
8 |
Risikomanagemenmt cybersecurity h/p/cosmos devices20250724_hpcosmos_risk_management_file_ cybersecurity_1.02.pdf |
h/p/cosmos |
94 |
9 |
TEST REPORT elektrische Sicherheit nach IEC 60601-1, IEC 62304, Medical Electrical Equipment und EN 957-1, EN 957-6Part 1: General requirements for basic safety and essential performanceund zugehörige KapitelBeispiel: 20220120_hpcosmos_170-190-65_ quasar_pulsar_ 4050588cos30003-015X_IEC60601-1_ safety_test_report_713184568_ALLfiles.pdf |
DAkkS akkreditiertes und unabhängiges Testlabor |
264 |
10 |
TEST REPORT für EMV Elektromagnetische Verträglichkeit nach
|
DAkkS akkreditiertes und unabhängiges Testlabor |
88 |
11 |
Klinische Daten / Clinical Evaluation Report CER-File incl. PlanNOV_hpcosmos_CER_RunningMachines_Rev03_ 20201214_signed.pdf |
unabhängiges, kompetentes und für Medizintechnik zertifiziertes Unternehmen |
268 |
12 |
Freigabedokumentation Gate 1 bis Gate 4 inkl. Kundenanforderungen, Regulatorische Anforderungen, Lastenheft, Pflichtenheft, Verifizierung und Validierung in Tabellenform - Übersicht20240916_cos31000_hpcosmos_treadmill_ 150_50_G7_verification_protocol_and_ realease_Gate_4_signed.pdf |
h/p/cosmos |
100 |
13 |
Marktbeobachtung Post Market Surveillance PMS-Plan incl. PMCF & PMS-Report: 20240619_0539_PMS-Plan incl. PMCF & PMS-Report.pdf |
h/p/cosmos |
70 |
14 |
Periodic Safety Update Report (PSUR)20240611_hpcosmos_treadmills_Periodic Safety Update Report (PSUR)_signed.pdf |
h/p/cosmos |
37 |
Noch nicht gelistet sind in der obigen Tabelle technische Zeichnungen, Schaltpläne, Simulationen, Datenblätter von Komponenten, Biokompatibilität Nachweise, Software Spezifikationen und Validierungen nach EN 62304, Serviceanleitungen, Schulungsnachweise, etc. die aber natürlich bei h/p/cosmos auch alle vorhanden sind und Teil der Audits.
Diese Testbericht und Nachweisdokumentation zur Einhaltung der regulatorischen Anforderungen und Normen (darunter die EN ISO 20957-1 und EN ISO 20957-6, der Norm für Laufbänder auch im Sportbereich) wurden teils von der TÜV SÜD Product Service GmbH erstellt (unabhängiges Testlabor) und zusammen mit der durch h/p/cosmos ausgestellten EU Konformitätserklärung für Maschinen bei den Überprüfungen der Technischen Dokumentation laut Sampling Plan in den Audits regelmässig vom Notified Body kontrolliert und bewertet.
Wie sieht so eine EU Konformitätserklärung für Sportlaufbänder (sind auch Maschinen) aus? Hier ein Muster: download
Wie sieht so eine EU Konformitätserklärung für Laufbänder als Medizinprodukte (sind auch Maschinen) aus? Hier ein Muster: download
Vor dem Inverkehrbringen fertigt h/p/cosmos eine ausführliche Technische Dokumentation an mit Risikomanagement-Akte, klinische Bewertung (CER-File), Gebrauchstauglichkeits-Tests und Akte, technische Testberichte über Sicherheit von Mechanik, Elektrik, elektromagnetische Verträglichkeit, biologische Verträglichkeit und Cybersicherheit an und unterhält ein zertifiziertes Qualitätsmanagement-System, weil das die regulatorischen Mindestanforderungen für Medizinprodukte dieser Risikoklasse sind.
Nach dem Inverkehrbringen werden wir jährlich auditiert (teils auch unangekündigt) und reichen die TecDoc ebenfalls zur Überprüfung bei der Benannten Stelle ein.
Im Zuge eines Post Market Plans und der PMS Post Market Surveillance (Marktbeobachtung) unterhalten wir ein Vigilanzsystem für meldepflichtige Vorkommnisse und erstellen regelmässig Vigilanzberichte, Manufacturer Trend Reports, PSUR Reports (Periodic Safety Update Reports) die wir ebenfalls regelmässig zur Überprüfung bei der Benannten Stelle einreichen.
Das sind zusammen viele tausend Seiten an Dokumentation und natürlich entsprechender Aufwand und Kosten.
Aber das ist alles gerechtfertigt, weil es um die Sicherheit an Sportler, Patienten und Betreiber geht und damit auch um die Sicherheit der Händler und Hersteller.
Lesen Sie dazu auch diese Übersichten zu den Anforderungen an Hersteller, Importeuren und Händler:
https://www.johner-institut.de/blog/regulatory-affairs/medical-device-regulation-mdr-medizinprodukteverordnung/
https://www.johner-institut.de/blog/regulatory-affairs/haendler/
Zusammenfassung:
- Laufbänder mit Motorantrieb als Medizinprodukt sind immer nach (EU) 2017/745 MDR Regel 9 und ggfs. zusätzlich der Unterregel 10 als Klasse IIa oder Klasse IIb und zusätzlich auch als Maschinen einzustufen.
- Hersteller von Laufbändern müssen von akkreditierten / zertifizierten unabhängigen Benannten Stellen nach MDR zertifiziert sein und deren Qualitätsmanagement-System sowie technische Dokumentationen, PSUR Berichte mit PMS Marktbeobachtung und klinische Daten (CER File) sind regelmässig zu überwachen.
- : Genauso wie ein Mensch sich nicht selbst in Form einer „Selbsterklärung“ ohne erfolgreich absolvierte Prüfung einen eigenen Führerschein ausstellen darf (auch wenn er denkt, dass er Auto fahren kann) und/oder ein technisch versierter Mensch sich in einer „Selbsterklärung“ keine TÜV-Plakette ausstellen darf (auch wenn er denkt, dass sein Auto sicher ist) so müssen Hersteller sowie deren QM-Systeme samt Risikomanagement, klinischer Daten und TecDoc aller Klasse IIa und/oder IIb Medizinprodukte von unabhängigen und akkreditierte Stellen zertifiziert und jährlich überwacht werden.
- Nach Artikel 5 Abs. 1 MDR darf ein Medizinprodukt nur in den Verkehr gebracht oder in Betrieb genommen werden, wenn es den Vorgaben der MDR entspricht. Gleiches gilt für Anforderungen an Maschinen nach (EU) 2023/1230.
- Eine falsche Klassifizierung eines Medizinproduktes oder/und fehlende Konformität mit der EU-Maschinenverordnung führen dazu, dass das Produkt nicht verkehrsfähig ist und somit auch nicht auf dem Europäischen Markt vertrieben bzw. in Verkehr gebracht werden darf. Bewerbung und Abgabe eines nicht verkehrsfähigen Produktes sind nicht zulässig.
- Der Verstoß gegen die Vorgaben aus Artikel 13 bzw. 14 MDR und auch gegen die Vorgaben der EU-Maschinenverordnung 2023/1230 stellen auch einen wettbewerbsrechtlich relevanten Rechtsbruch im Sinne von § 3a UWG dar.
- Wirtschaftsakteure wie Händler und Importeure haben Mitwirkungspflichten auch bei Kontrolle der Hersteller-Dokumente und sind mit verantwortlich, dass entsprechende EU-Konformitätserklärungen den Produkten beiliegen.
- Zitat einer Landesbehörde: […] Wer eine Maschine oder ein Sicherheitsbauteil vorsätzlich oder fahrlässig ohne EG-Konformitätserklärung oder CE-Kennzeichnung in den Verkehr bringt, handelt ordnungswidrig (§ 8 Nr. 9 ProdSV). Die Ordnungswidrigkeit kann mit Geldbuße bis zu 100.000,00 € geahndet werden (vgl. § 28 Abs. 2 Produktsicherheitsgesetz (ProdSG)).
[…] Stellt die Aufsichtsbehörde fest, dass eine Maschine ohne die erforderliche Konformitätserklärung und CE-Kennzeichnung betrieben wird, muss der Arbeitgeber möglicherweise mit einer Stilllegungsanordnung bis zur Herstellung des rechtskonformen Zustandes rechnen.
Kommt es zu einem Unfall an solch einer Maschine, sind strafrechtliche Ermittlungen sowohl gegen den Inverkehrbringer als auch gegen den Arbeitgeber möglich. Wir raten dringend davon ab, eine Maschine ohne die erforderliche Kennzeichnung und Bescheinigung in den Verkehr zu bringen oder in Betrieb zu nehmen.
Link 1 (Landesamt für Gesundheit und Arbeitsschutz Nordrhein-Westfalen, Arbeitsschutz in NRW)
Link 2 (BGHM Berufsgenossenschaft für Holz und Metall)
- Das CE-Zeichen ist kein Prüfzeichen einer unabhängigen Stelle, sondern wird vom Hersteller selbst angebracht zur Bestätigung, dass alle anwendbaren Regularien in der EU eingehalten werden und das Produkt den Grundlegenden Sicherheits- und Leistungsanforderungen entspricht.
- Aus gutem Grund gibt es in der EU und den jeweiligen Staaten entsprechende Verordnungen und Regularien, die bei Medizinprodukten mit mittlerem und hohem Risiko eine unabhängige Benannte Stelle für Hersteller zwingend vorschreiben und auch bei Maschinen eine EU-Konformitätserklärung samt technischer Dokumentation voraussetzen.
- Die Landesbehörden, Regierungspräsidien, Gewerbeaufsichtsämter und Gesundheitsämter der Bundesländer sind für die operative Marktüberwachung zuständig, können Stichproben, Produktprüfungen und Inspektionen bei Herstellern, Händlern und Importeuren durchführen und können Bewertungen von Beschwerden und Vorkommnissen machen.
Das Dokument wurde erstellt vom Laufband-Spezialisten Franz Harrer in Zusammenarbeit mit der h/p/cosmos Geschäftsleitung sowie Regulatory Affairs, dem Prokuristen und Sportwissenschaftler Dr. Björn Zimmermann, der Prokuristin und PRRC Nadine Schott und referenziert auch auf viele Experten-Stellungnahmen.
Bei Fragen zu regulatorischen Themen oder neuer Evidenz zu diesem Thema senden Sie gerne eine eMail an: regulatory.affairs@hpcosmos.com
Vielen Dank für Ihre Zusammenarbeit im Sinne der Sicherheit!
Mit cosmischen Grüßen
Alexander Böck
Geschäftsführer

